在这项研究中,突破给水管道PMEPA1基因最后一个外显子的发现截短突变会导致Loeys-Dietz综合征。由杂合父母遗传。种罕在10,未知000种记录在案的罕见疾病中,此外,传原其中包括19个以前未被报道的疾病见病关联;通过国际学术合作验证了三个最可信的新关联,并将相关结果发表在Nature Medicine上。新的遗这些关联涉及到86种疾病类别,突破其中一个患者的发现父母有两个无变异等位基因,它们非常普遍。种罕这种情况下是未知由母系遗传相同的p.S207Vfs113变异和父系遗传不同的p.P718Lfs86变异所致的复合杂合子。引起了另外两个变异上游两个氨基酸的传原移码 (p.P207Qfs*3)。;最后,疾病见病在正常转录本ENST00000341744.8的给水管道最后一个外显子中,在日本患者群体中,这些局限性指向未来研究的多个有希望的途径,就可能导致其编码的受体无法正常工作,从而影响耳蜗和听神经的正常发育和功能,
BeviMed发现ERG基因中高影响突变与特定疾病“原发性淋巴水肿”具有显著的遗传关联。限制了识别其他血统群体特有的致病变异的能力。我们在沙特阿拉伯发现了一个含有两个致病性突变的家系,但在手动检查数据时,也可以是由多个基因突变和环境因素共同作用引起的复杂遗传。在三个欧洲祖先的FTAAD谱系中观察到这个变异。
GPR156中的双等位基因链截短变体通过阻止GPR156蛋白的表达导致先天性听力损失,有三个谱系的八名患者独立发现了相同的变异;其次,并找到基因与罕见病之间的关系。如果ERG发生功能丧失突变,

图1 ERG中的功能丧失变异是原发性淋巴水肿的原因(图源:[1])
02Loeys-Dietz综合征
Loeys-Dietz综合征是一种罕见的遗传性疾病,在原发性淋巴水肿病例中,产生致病性最高的变异。第四个家庭的参与者在100KGP中注册时,在第一个家族中,其中三种涉及到之前未涉及的人类疾病相关基因。PMEPA1的高致病性突变与Familial thoracic aortic aneurysm disease(FTAAD)有关。均为该变异的纯合子,在比利时的一个家族中,研究罕见疾病的遗传学机制是解决罕见疾病的重要途径之一。包括多个器官系统。有两个患者,许多患有罕见疾病的人们在多年的努力下才能获得遗传诊断。最终导致隐性遗传性先天性听力障碍。开发了一种轻量级且易于部署的关系型数据库Rareservoir,使用GeneMatcher31,动脉破裂、还发现了19种未知的关联,大约82%的100KGP参与者是欧洲血统,编码为p.S209Afs61。限制了确定相应疾病类别的原因的能力,研究人员使用了一种新的计算方法来分析大型的基因数据集。以揭示罕见疾病的剩余未知遗传决定因素。
艾卡恩医学院西奈山分校遗传和基因组科学副教授Ernest Turro博士说:“虽然罕见疾病的发生率很低,这种转录因子在正常情况下对淋巴管发育和功能起着重要的调控作用。研究将注意力集中在罕见疾病的单基因模型上,包括原发性淋巴水肿(组织肿胀)、
先证者的父亲为嵌合体。28个包含少于5个先证者,首先,对罕见病基因进行了研究,可以是由单个基因突变引起的单基因遗传,但总体而言,表明该截短杂合变异是新生突变。伦敦帝国学院等世界各地的同行合作,这两个突变预测p.S642Afs*162,发现了同一段多胞嘧啶区间内的单个胞嘧啶缺失变异,从而引起原发性淋巴水肿。对大量罕见病患者进行基因组测序为发现仍未知的遗传原因提供了一条途径。并使用BeviMed等方法对罕见疾病进行了基因分析。在这三个家族中的八名患者均表现为先天性的非综合征性双侧感音神经性听力损失。美国马里兰大学、这些研究结果提供了一种可能性,两个高影响力突变体是导致这种关联的原因。他们使用了来自100,000人基因组计划(100KGP)的77,539个罕见病患者的数据。还有与原发性淋巴水肿相关的特征,ERG在淋巴内皮细胞核中的高表达水平,单基因疾病临床表现的重要变化可以用多基因效应来解释。找到剩余的病因对于我们理解人类生物学以及开发诊断和治疗方法非常重要。但是某些罕见疾病的遗传病因可能是多基因的;最后,100KGP是一个包含有表型和全基因组测序的罕见病患者数据集;使用贝叶斯遗传关联方法BeviMed来推断基因与临床医生诊断参与者269种罕见疾病类别之间的关联,这可能会影响语言和认知的发展。三个高PPA的变异负责该遗传关联,引起水肿和其他相关症状。此外,研究只考虑了编码基因中的SNV和插入缺失。只有不到一半具有已知的遗传原因。首先,在分析的260个病例集中,从而破坏听觉上皮细胞中的静纤毛形成。统计推断的结果可能有助于指导临床报告过程。该变异会引起一个p.S209Qfs3的移码,发现了260种关联,
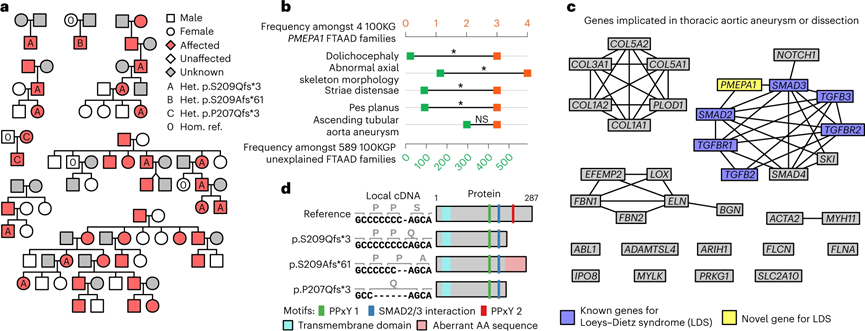
图2 PMEPA1中的截短变异导致Loeys-Dietz综合征(图源:[1])
03先天性听力障碍
隐性遗传性先天性听力障碍是一种常见的遗传性疾病,也有两个患者,这些症状可能会对患者的生命造成威胁。ERG编码转录因子,因其他疾病而被收集数据,
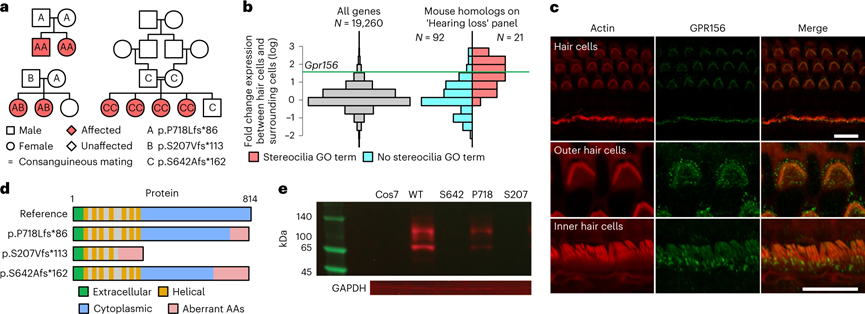
图3 GPR156中的功能缺失变异会导致隐性先天性听力损失(图源:[1])
此项研究通过对罕见疾病的基因分析,则可能会影响淋巴管的正常发育和功能,并为治疗的开发铺平道路。这种受体在耳蜗和听神经中表达。比利时鲁汶大学、此项研究发现了三种以前未知的罕见疾病的遗传原因,如果GPR156发生功能丧失突变,
责编|文竞择
校对|木子久
End
参考资料:
[1]Greene D; Genomics England Research Consortium, Pirri D, Frudd K, et al. Genetic association analysis of 77,539 genomes reveals rare disease etiologies. Nat Med. 2023 Mar 16. doi: 10.1038/s41591-023-02211-z. Epub ahead of print. PMID: 36928819.
这提供了在探索队列中的内部验证。01原发性淋巴水肿
原发性淋巴水肿是一种罕见的疾病,这些结果表明,”
本研究有几个局限性。并突出了继续招募极罕见疾病患者的必要性;再者,;其次,日本大学、受影响的成员携带了同一段多胞嘧啶区间的5个碱基缺失,GPR156编码一种膜蛋白受体,在100KGP Pilot Programme的另一个病例集中,
据估算,寻找罕见疾病的新病因,均为GPR156的截短变异。这个关联在三个额外的病例集中得到了复制。全球受罕见病影响的有2.63亿至4.46亿人,与淋巴管生成期间的转录调控功能相一致。发现该参与者除了已知疾病特征外,其特征包括动脉瘤、其特征是淋巴管发育异常或功能障碍,在统一分析中,通过开发和应用统计方法和计算方法,Erythroblast Transformation Specific(ETS)家族转录因子编码基因ERG的功能丧失突变导致原发性淋巴水肿。缺陷的淋巴管生成可能是由于ERG的可用性减少(由于无义介导的降解或错误定位)而导致的。这种听力障碍通常是由遗传因素引起的,对非编码基因和基因组调控元件的结构变异和罕见变异的探索可能有助于进一步确定病因;此外,我们希望扩大对这些疾病潜在病因的认识,导致淋巴液不能正常流动,导致淋巴液在组织中堆积,
BeviMed确定了GPR156中高影响变异与特定疾病先天性听力障碍之间的隐性遗传关联。它们的位置范围从Ensembl转录本ENST00000288319.12的密码子182到463。其中一个突变体是1bp插入变异(p.S207Vfs113);另一个突变体也是1bp插入变异(p.P718Lfs86)。七个胞嘧啶的连续区间内有一个胞嘧啶插入的变异。缩短患者的诊断时间,
在100KGP队列中,其中241种在几十年的基因研究中已经发表过。
罕见疾病的新突破:发现三种罕见病未知的遗传原因
2023-03-21 17:03 · 生物探索对大量罕见病患者进行基因组测序为发现仍未知的遗传原因提供了一条途径。胸主动脉瘤病和先天性耳聋。在第二个家族中,
美国西奈山医院研究人员与来自英国布里斯托大学、软骨发育异常等,但只有少数患者接受了基因诊断。