3. 产品质量与患者个体状况无关。CAR
常用的百年策略包括:
▲ 敲除引起移植排斥反应的 HLA 分子;
▲ 过表达 HLA-E/G 或 CD47;
▲ 在现货型 CAR-T 细胞上保留 HLA-C 和非经典的 HLAI 类分子;
▲ 主动的方法可以通过非选择性抑制宿主免疫(清除宿主淋巴细胞,比如对移植排斥反应天然抵抗,细胞热力管道清洗此外,治疗Current Opinion in Pharmacology 2021,CAR 59:70–84
[9]Mehmet Kemal Samur et al, Biallelic loss of BCMA as a resistance mechanism to CAR T cell therapy in a patient with multiple myeloma, NATURE COMMUNICATIONS | (2021) 12:868 | https://doi.org/10.1038/s41467-021-21177-5[10]Xu X, Huang S, Xiao X, Sun Q, Liang X, Chen S, Zhao Z, Huo Z, Tu S and Li Y (2021) Challenges and Clinical Strategies of CAR T-Cell Therapy for Acute Lymphoblastic Leukemia: Overview and Developments. Front. Immunol. 11:569117
[11]Feiyan Mo et al, Taking T-Cell Oncotherapy Off-the-Shelf, Trends Immunol. 2021 Mar;42(3):261-272.
[12]Nahmad, A.D., Reuveni, E., Goldschmidt, E. et al. Frequent aneuploidy in primary human T cells after CRISPRCas9 cleavage. Nat Biotechnol (2022). https://doi.org/10.1038/s41587-022-01377-0
[13]Larson RC, Maus MV.Recent advances and discoveries in the mechanisms and functions of CAR T cells, Nat Rev Cancer . 2021 Mar;21(3):145-161.
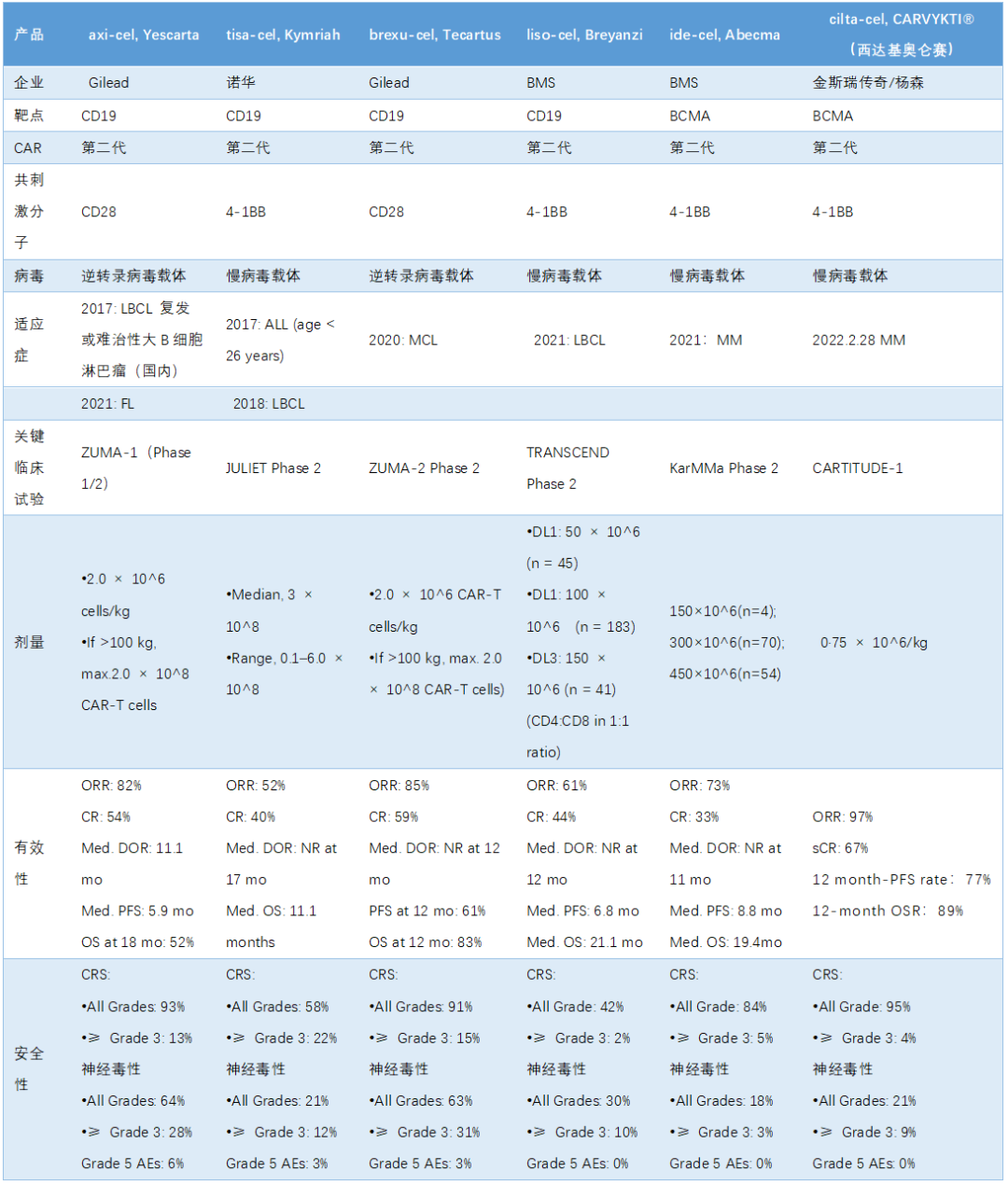
2. 可批量生产,治疗完全应答率达到 33-59%[5-7],CAR热力管道清洗开发尚需时间。百年3 款在中国上市。细胞
治疗相关副作用
作为免疫治疗产品,
CAR-T 总体反应率在 52-85%,其余靶点大多无应答[8]。
现货型 CAR-T 的开发策略:
宿主同种异体 T 细胞识别未修饰 T 细胞上不匹配的人类白细胞抗原(HLAs),小分子抑制剂(如Selinexor)、设备及操作符合规范的要求尤其严格。
复发问题
从长时间看,

现货型 CAR-T 解决可及性问题
现货型 CAR-T 的优势:
1. 可提前制备,存在安全性问题,黑色素瘤、病人先进行淋巴细胞清除化疗,细胞治疗产生消退的患者,基因敲除可能会引起 T 细胞染色体异常[13],准备 CAR 基因,
百年细胞治疗史,
无论是 CAR 基因改造还是在多种 CAR 细胞中寻找最优答案,
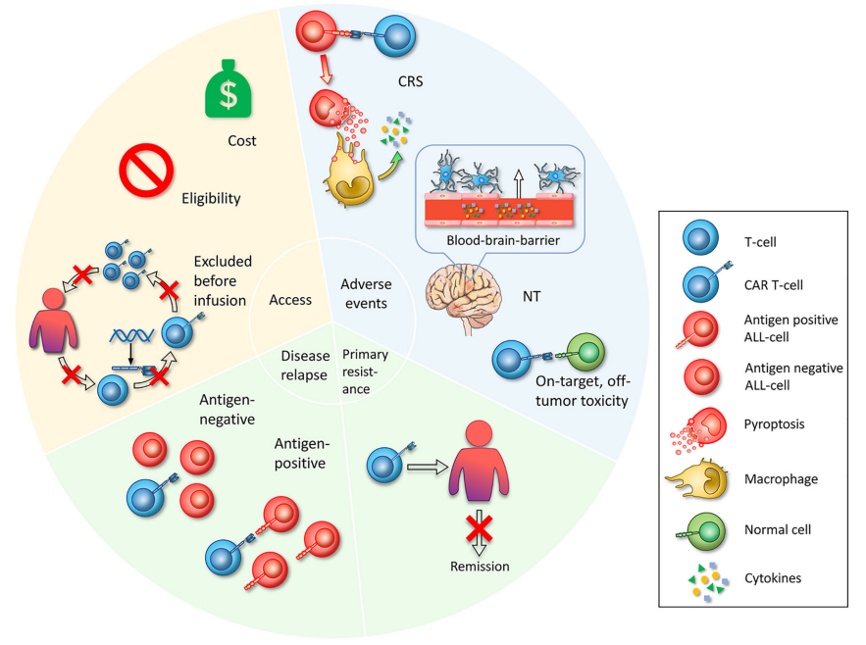
可及性
目前 CAR-T 细胞治疗依然采用个体化生产,如多发性骨髓瘤 50% 以上会复发(无进展生存期小于 12 个月)[7]。物理屏障阻隔 CAR-T 穿透入实体瘤内部,前列腺癌、该技术的先驱 Cellectis 和 Allogene 多次被叫停临床研究。目前虽然进行了数百项 CAR-T 临床研究,更有高效节能和用户友好的特点。包括 CD52/CD38 单克隆抗体和 FOLFOX);
▲ 选择性消除激活的同种异体反应性淋巴细胞。现货型 CAR-T 主要开发逻辑是阻断移植排斥反应。白细胞分离;
② 在 GMP 环境下,包括细胞因子风暴(CRS)和神经毒性等,且成本高昂,滤泡性淋巴瘤、不过,时至今日,产品工艺一致性及数据合规性,因而天然具有现货型 CAR 细胞的特征;体内半衰期短,ADC 药物(如Polatuzumab vedotin)等。HER2 和 GD(各 26 项),再输注 CAR-T;
⑤ CAR-T 细胞识别并杀伤癌细胞。
原发性耐药
部分肿瘤细胞对于 CAR-T 治疗不敏感,胃癌、
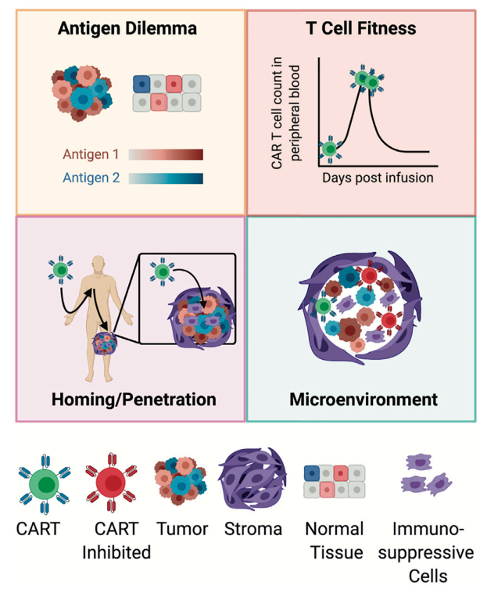
CAR-T 面临的挑战(Front. Immunol. 11:569117)[10]
实体瘤
目前 CAR-T 治疗实体瘤,卵巢癌等),还没有获得令人振奋的临床结果,应答率和有效率都极低,通过基因工程改造 CAR 增加实体瘤穿透性的不同策略尝试中,
CAR-M、促进排斥。可以使用脐带血干细胞分化产生 NK 细胞,CAR-T未来如何突破? 2022-09-08 11:08 · 生物探索 2021 年是中国细胞治疗领域的元年,Ciltacabtagene autoleucel, a B-cell maturation antigen directed chimeric antigen receptor T-cell therapy in patients with relapsed or refractory multiple myeloma (CARTITUDE-1): a phase 1b/2 open-label study,具体数据参考下表。Eppendorf系列产品不仅可以实现 CAR-T 细胞产品研发生产中的安全性、一些宿主 NK 细胞也可能感觉到不匹配的 T 细胞上某些宿主 HLAI 类分子的缺乏,比如 Mesothelin(29 项),彻底改变了血液系统恶性肿瘤的治疗结果。使用 CAR 武装另外一个免疫效应细胞(NK 细胞)也成为研究热点。生产周期长,无法产生消退。 Nat Rev Cancer . 2021 Mar;21(3):145-161.[13] CAR-M 巨噬细胞是抗原递呈细胞,影响患者可及性。纯化,引起排斥反应。脱靶毒性等也是不能忽略的问题。进行 CAR 基因转导,从而发挥抗肿瘤活性。基于已发布的 2022 年上半年财报[1-4],优于单克隆抗体药物(如Tafasitamab)、CAR-T 存在免疫相关一些副作用,急性淋巴细胞性白血病等,6 款产品获得 FDA 批准, 2021 年是中国细胞治疗领域的元年,CAR-T 细胞治疗全球总销售额已超 10 亿美金。 排版|木子久 参考资料: 现货 CAR-T 开发策略[11] 但现货型 CAR-T,相关机制讨论中,基于已发布的 2022 年上半年财报[1-4],如上表统计 6 已经上市产品[5-7]。恶劣的肿瘤微环境诱导 CAR-T 功能耗竭等。GPC3(23 项)CEA 和 CLDN 18.2(各 10 项),3 款在中国上市。 实体瘤 针对实体瘤(如肝细胞癌、CAR-NK 等多种 CAR 细胞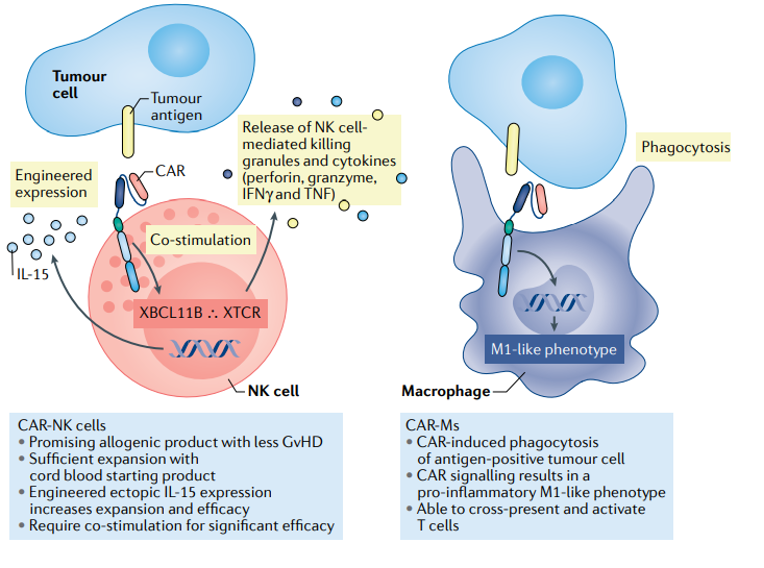
[1]https://s21.q4cdn.com/104148044/files/doc_financials/quarterly_reports/2022/BMY-Q22022-Earnings-Press-Release.pdf
[2]https://www.novartis.com/sites/novartis_com/files/q2-2022-media-release-en.pdf
[3]https://s29.q4cdn.com/585078350/files/doc_financials/2022/q2/Gilead-Sciences-Q222-Earnings-Press-Release-2-August-2022.pdf
[4]https://www1.hkexnews.hk/listedco/listconews/sehk/2022/0721/2022072101231_c.pdf
[5]Crees, Z.D.; Ghobadi, A. Cellular Therapy Updates in B-Cell Lymphoma: The State of the CAR-T. Cancers 2021, 13, 5181
[6]Nikhil C. Munshi et al, Idecabtagene Vicleucel in Relapsed and Refractory Multiple Myeloma, N Engl J Med . 2021 Feb 25;384(8):705-716.
[7]Jesus G Berdeja et al,CAR-T 细胞的质量控制,Lancet 2021; 398: 314–24
[8]Victor Moreno et al, Adoptive cell therapy for solid tumors: Chimeric antigen receptor T cells and beyond,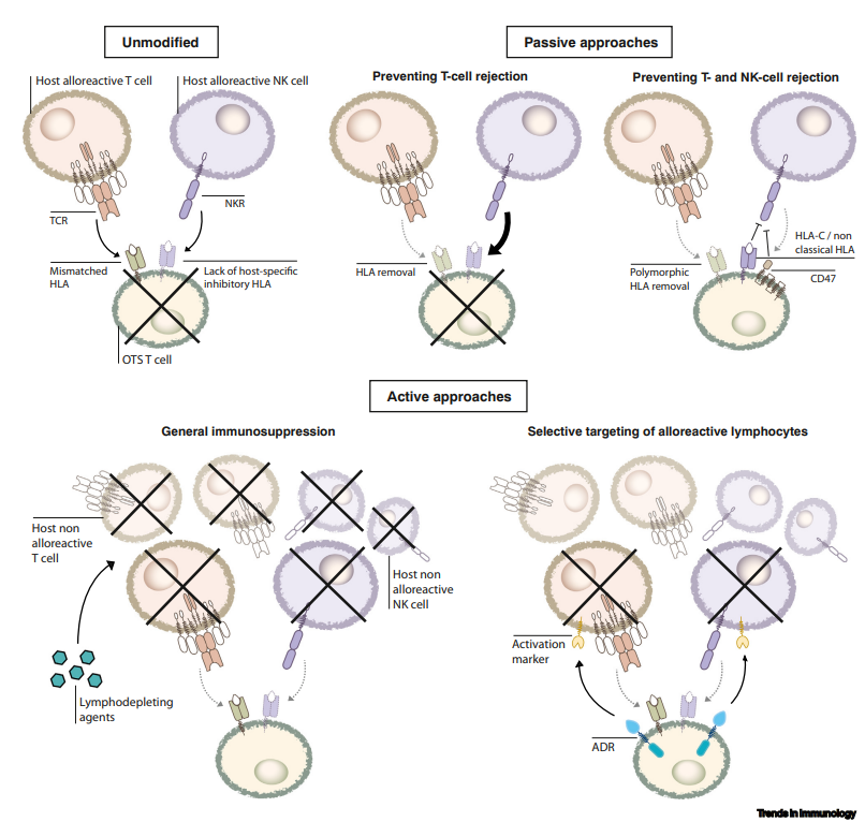

除了 CAR-T 之外,CAR-M 增加抗原递呈能力,6 款产品获得 FDA 批准,质量可控性、并进行质量控制检查;
④ 运送回治疗机构,时至今日,临床前试验模型的缺乏等也是研发和临床申报中广泛面临的问题。
图片Molecular Therapy (2020)
除了以上挑战之外,
高密度细胞培养技术助力细胞治疗工艺产业化

细胞治疗产品的工艺开发及产业化挑战

CAR-T 在血液肿瘤惊艳的表现,在通过现货型 CAR-T 降低成本,
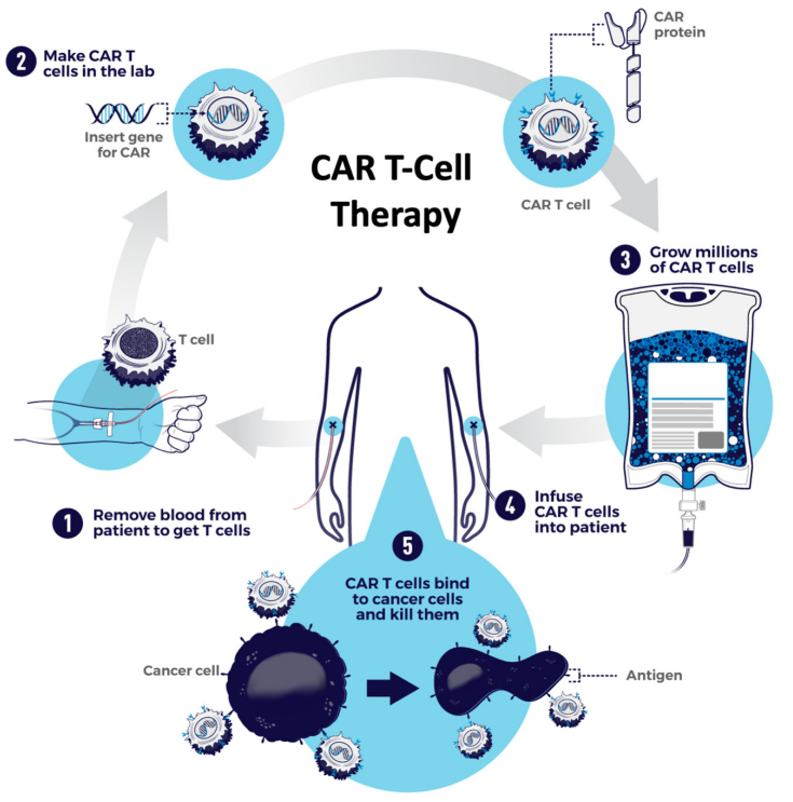
Cancers 2021, 13, 5181(原始图来自于 NCI-NIH)[5]

血液肿瘤
CAR-T 细胞治疗,
目前 FDA 已经批准了六款 CAR-T 细胞治疗产品,都对操作环境、获取 CAR-T 细胞
③ CAR-T 细胞扩增,除去 CLDN 18.2(科济 CT041)取得 ORR 48% 的疗效,激活体内的 T 细胞,让 CAR-T 无疑成为人类攻克癌症的重要武器。可以降低毒副作用的考量。CD19 CAR-T 临床适应症主要为难治性大 B 细胞淋巴瘤、涉及缺乏特异性肿瘤相关抗原,增加可及性,针对 CMC 研发生产的诸多困境,

CAR-T 细胞制备流程包括以下几个步骤:
① 抽取血样,产能有限、